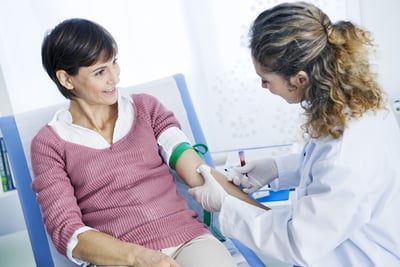
Estudio: Una nueva prueba de sangre puede ayudar a detectar el cáncer de mama en fase inicial en pacientes que tienen mayor riesgo de recaída
¿Cuáles pacientes con cáncer de mama en fase inicial corren mayor riesgo de tener una recaída? Las pruebas para predecir el riesgo de recaída serían útiles para encontrar a personas que necesitan más supervisión después del tratamiento, así como para identificarlas y tratarlas oportunamente. Este estudio analizó si una prueba de sangre para detectar ADN tumoral (llamado ADN tumoral circulante o ctDNA) es útil para identificar a personas con riesgo de recaída con más anticipación que en la práctica clínica actual. (Publicado 4/11/19)
RELEVANCIA
Este artículo es de mayor interés para: Personas con cáncer de mama en fase inicial.
También es de interés para:
- Personas con cáncer de mama ER/PR+
- Personas con cáncer de mama HER2+


Relevancia: Media-alta


Validez científica: Media-alta

Línea de tiempo: Investigación en humanos
¿De qué se trata el estudio?
Si una prueba de ctDNA puede ser útil para detectar a pacientes que tienen un mayor riesgo de una recaída.
¿Por qué es importante este estudio?
Este estudio analiza si una prueba de detección de ctDNA puede predecir cuáles pacientes con cáncer de mama en fase inicial tendrán una recaída. Una prueba que predice el riesgo de una recaída antes de que el cáncer sea clínicamente detectable podría permitir brindar tratamiento temprano o quizá diferente, y puede aumentar el índice de supervivencia.
Resultados del estudio
- La detección de ctDNA en la sangre fue un sólido indicador de riesgo de recaída entre las participantes del estudio. Las pacientes a quienes se les detectó ctDNA después del tratamiento inicial fueron 25 veces más propensas a tener una recaída que las pacientes a quienes no se les detectó ctDNA después del tratamiento inicial.
- La detección de ctDNA fue útil para predecir el riesgo de recaída en todos los subtipos de cáncer de mama analizados (HER positivo, HER negativo y triple negativo).
- La detección de ctDNA antes de una cirugía u otro tratamiento también se relacionó con el riesgo de recaída. Las pacientes a quienes se les detectó ctDNA antes del tratamiento fueron casi 6 veces más propensas a recaer que las pacientes a las que no se les detectó al momento del diagnóstico.
- Era más probable detectar ctDNA en metástasis en lugares del cuerpo distintos del cerebro que en metástasis cerebral. En este estudio, el ctDNA no ayudó a identificar a pacientes cuya única metástasis ocurrió en el cerebro.
- Si bien el ctDNA parece ser un buen indicador de cuáles pacientes sufrirán una recaída, a 25 % de las pacientes que recayeron no se les detectó ctDNA en este estudio. La ausencia de ctDNA no descarta el riesgo de recaída.
¿Qué significa esto para mí?
La mayoría de las pacientes con cáncer de mama en fase inicial responderán bien al tratamiento sin tener una recaída. No obstante, es posible que algunas recaigan. Por esta razón, las recomendaciones actuales consiste en asistir a consultas de seguimiento tras el tratamiento. Detectar el riesgo de recaída de manera temprana puede proporcionar más opciones de tratamiento a las pacientes. Una vez que termine su tratamiento, es importante que hable con su doctor acerca del seguimiento, incluyendo:
- la frecuencia de las consultas de seguimiento
- a qué profesionales de la salud debe acudir
- qué pruebas se solicitarán
- los síntomas que debe notificar a su doctor
Las investigaciones sobre la detección de ctDNA como técnica para supervisar las recaídas están en curso. Si bien la prueba es prometedora, aún no ha demostrado que influye en los índices de supervivencia en las pacientes. Se requieren pruebas de detección de ctDNA de seguimiento más extensas para determinar si esta información puede ser útil desde el punto de vista clínico.
Referencias
Garcia-Murillas I, Chopra N, Comino-Méndez, et al. “Assessment of molecular relapse detection in early-stage breast cancer”. JAMA Oncology. 5(10):1473-1478. Publicado en línea el 1 de agosto de 2019. doi:10.1001/jamaoncol.2019.1838.
Declaración de divulgación: FORCE recibe financiamiento de patrocinadores de la industria, que incluyen a empresas que producen medicamentos, pruebas y dispositivos contra el cáncer. Todos los artículos de XRAY se redactan de manera imparcial respecto a cualquier patrocinador y se someten a revisión por parte de los miembros de nuestro Consejo asesor científico antes de su publicación con el fin de garantizar la integridad científica.
Compartan sus opiniones sobre esta revisión de XRAY respondiendo nuestra breve encuesta.
- ¿Dado el tipo de cáncer de mama que padezco, ¿cuáles son las posibilidades de una recaída?
- ¿Cuál es la mejor manera de monitorearme para detectar una recaída?
- ¿Cuáles son los signos o síntomas de recaída para el tipo de cáncer de mama que padezco?
- ¿Debe hacerse una secuenciación del ADN del tumor primario?
- ¿Es útil monitorear el ctDNA o las células tumorales circulantes en mi caso?
- ¿Con cuánta frecuencia debo hacerme exploraciones de seguimiento o mamografías?
- ¿Me puede proporcionar un plan de atención para la etapa de supervivencia?
ANÁLISIS DETALLADO DE LA INVESTIGACIÓN
Antecedentes del estudio
De las mujeres con cáncer de mama en etapa inicial, 95 % no mostraban metástasis al momento en que se les hizo el diagnóstico. Muchas de estas pacientes no sufrirán una recaída. La tasa de supervivencia de 5 años para las mujeres con cáncer de mama local es 98 % y, para las que padecen cáncer de mama regional, 88 %.
La recaída se atribuye a pequeños grupos de células cancerosas que permanecen después del tratamiento (se le llama “enfermedad mínima residual” o “MRD”, por sus siglas en inglés). Estas células son tan pocas que es difícil observarlas. Cuando estas células cancerosas migran a otras partes del cuerpo se llaman metástasis. La detección oportuna y el tratamiento temprano es fundamental para las pacientes que sufren recaídas.
¿Cuál es la mejor manera de predecir quién recaerá y quién no? Es posible que esas células cancerosas restantes deriven en ADN tumoral en la sangre de las pacientes, conocido como ADN tumoral circulante o ctDNA. Es posible que las células cancerosas en las pacientes con ctDNA en la sangre crezcan posteriormente, hasta que sean clínicamente detectables o causen síntomas, es decir, que haya una recaída de su cáncer primario.
Los investigadores de este estudio querían saber si la detección de ctDNA predecía correctamente la probabilidad de recaída en las pacientes con cáncer de mama. La clave para usar el ctDNA es encontrar una alteración que ocurrió solo en el tumor mientras crecía (no una alteración heredada). Para hacer esto, se hace una secuenciación del ADN del tumor primario para encontrar alteraciones que difieren del ADN no tumoral. Estas alteraciones actúan como un distintivo de las células tumorales.
Los investigadores que participaron en este estudio querían saber
Si el ctDNA en la sangre indica que existe un mayor riesgo de recaída. La pregunta que persiste es si la detección de ctDNA puede ser un método útil clínicamente para identificar a pacientes con mayor riesgo de una recaída.
Poblaciones que se analizaron en este estudio
Este estudio incluyó a 170 mujeres (mediana de edad de 54 años) de 5 hospitales del Reino Unido.
Todas las pacientes tenían cáncer de mama primario sin presencia de metástasis, de acuerdo con los métodos de monitoreo estándar.
Diseño del estudio
Este fue un estudio de seguimiento de grupos, realizado en más de un centro en Reino Unido, desde noviembre de 2011 hasta octubre de 2016. Todas las participantes tenían cáncer de mama en fase inicial. A 140 participantes se les dio tratamiento complementario (antes de la cirugía); otras 30 se sometieron a cirugía y a tratamiento complementario (después de la cirugía).
Para determinar si el ctDNA fue útil para predecir las recaídas, las muestras de sangre de cada participante se tomaron antes y después de su tratamiento inicial. Al momento de la cirugía, el ADN del tumor primario de cada participante se secuenció a fin de detectar alteraciones que identificaban de manera única las células tumorales. Se tomaron muestras de sangre de las pacientes cada 3 meses durante el primer año, y cada 6 meses en los años posteriores hasta por 5 años. Cada muestra se examinó en busca de ctDNA, y se recopilaron datos para verificar si las pacientes habían tenido o no una recaída.
A fin de tener suficientes cifras para comparar los diferentes subtipos de cáncer, el análisis de los datos del grupo de 101 participantes se combinó con los datos del estudio de viabilidad preliminar de 43 pacientes para dar un total de 144 pacientes, de las cuales, 29 sufrieron una recaída durante el estudio.
Resultados del estudio
De 170 pacientes que participaron en este estudio, en 101 se observó una alteración tumoral específica.
- Las 101 pacientes tenían al menos una alteración tumoral específica:
- 78 pacientes mostraron 1 alteración tumoral específica.
- 23 pacientes mostraron varias alteraciones tumorales específicas.
- 69 pacientes no mostraron alteraciones tumorales específicas.
En un promedio de 35 meses, se tomaron muestras de sangre y se recopilaron antecedentes personales de cáncer de las 101 participantes en las que se identificó alteración tumoral.
Las conclusiones principales incluyen:
1. La detección de ctDNA en la sangre fue un sólido indicador de recaída entre las participantes del estudio. Las pacientes a quienes se les detectó ctDNA después del tratamiento inicial fueron 25 veces más propensas a tener una recaída que aquellas que no.
Entre las 101 participantes de este estudio, la presencia de ctDNA en la sangre se relacionó con recaída.
- A 16 de 101 (casi 16 %) pacientes se les detectó ctDNA en la sangre.
- 9 tuvieron una recaída durante el estudio.
- 7 no habían tenido recaída al momento en que se publicó este estudio.
- En promedio, pasaron 38 meses entre el tratamiento o la cirugía inicial y la detección de ctDNA.
- 12 (casi 12 %) pacientes recayeron durante este estudio.
- A 9 se les detectó ctDNA antes de recaer (75 %).
- A 3 no se les detectó ctDNA (25 %).
2. La detección de ctDNA fue igualmente útil para predecir el riesgo de recaída de todos los subtipos de cáncer de mama analizados (HER positivo, HER negativo y triple negativo).
A fin de tener suficientes cifras para comparar los diferentes subtipos de cáncer, los datos del grupo de 101 participantes se combinaron con los datos del estudio de viabilidad preliminar de 43 pacientes para dar un total de 144 pacientes.
De estas 144 pacientes:
- 29 de 144 sufrieron una recaída.
- A 23 de 29 pacientes (79 %) se les detectó ctDNA antes de su recaída.
- A 6 de 29 pacientes (21 %) no se les detectó ctDNA antes de recaer.
- Entre estas 6 pacientes, todas tuvieron una recaída localizada:
- 3 solo en el cerebro
- 1 solo en el ovario
- 2 en un área cerca del tumor primario en el seno
- Entre estas 6 pacientes, todas tuvieron una recaída localizada:
- La detección de ctDNA se hizo 10.7 meses antes de la recaída clínica para todos los tipos de cáncer de mama.
3. La detección de ctDNA antes de la cirugía u otro tratamiento también se correlacionó con el riesgo de recaída.
- Se detectó ctDNA en 41 de 80 pacientes (51 %) en las muestras de sangre tomadas antes del tratamiento.
- Las pacientes a quienes se les detectó ctDNA antes del tratamiento fueron casi 6 veces más propensas a recaer que las pacientes a las que no se les detectó al momento del diagnóstico.
- La detección al momento del diagnóstico se relacionó con un tumor de mayor tamaño y grado.
4. Fue más probable detectar ctDNA en metástasis en lugares del cuerpo distintos del cerebro que en metástasis en el cerebro. En este estudio, las metástasis que solo se dieron en el cerebro no se detectaron por medio del ctDNA.
- Se detectó ctDNA en 22 de 23 pacientes (96 %) que recayeron cuando el sitio donde se dio la metástasis no fue el cerebro.
- Se detectó ctDNA en 1 de 6 pacientes (17 %) que recayeron cuando el sitio donde se dio la metástasis fue el cerebro.
5. Si bien el ctDNA parece ser un buen indicador de cuáles pacientes sufrirán una recaída, algunas pacientes a quienes no se les detectó ctDNA recayeron durante este estudio (es decir, carecer de ctDNA no significa que no habrá una recaída).
- Entre el grupo de 101 pacientes, a 3 de 9 (33 %) participantes que recayeron no se les detectó ctDNA.
- Entre el grupo combinado de 144 pacientes, a 6 de 29 (21 %) participantes que recayeron no se les detectó ctDNA.
Limitaciones:
Dado que este estudio se realizó solo en una región geográfica (Reino Unido), se desconoce si los resultados pueden generalizarse en relación con otras regiones y poblaciones.
Se identificaron alteraciones tumorales específicas en 101 de las 170 participantes. En el caso de 69 pacientes, no se registró la presencia o ausencia de ctDNA. En un entorno clínico, se pretenden identificar las alteraciones del tumor de una paciente determinada.
Aunque este estudio indica que la detección de ctDNA es un método prometedor para predecir quién necesitará más supervisión o tratamiento, la cantidad de participantes es reducida. Por otra parte, dos grupos de participantes, aquellas de este y del estudio de viabilidad preliminar, mostraron diferentes índices de recaída. Si bien se planeó combinar a estos grupos, esto puede representar tendencias desconocidas en ambos grupos. Es necesario un estudio más grande con un periodo más prolongado de seguimiento para evaluar si esta técnica es realmente útil en un entorno clínico y si ayuda a mejorar los resultados.
Entre las pacientes con metástasis en el cerebro, a ninguna se le detectó por medio de ctADN en este estudio. Esto indica que se necesitarán otras herramientas y una detección de ctDNA más exacta para supervisar las recaídas de este tipo.
Conclusiones
Si bien este método es prometedor, aún no se valida para uso clínico. Si se valida, la presencia de ctDNA puede ser útil para determinar tratamientos más oportunos antes de que aparezcan los síntomas de recaída. Sin embargo, como afirmaron los investigadores del estudio: “Los resultados que obtuvimos demuestran la validez clínica de dar seguimiento a la alteración de ctDNA, pero no demuestran la utilidad clínica. Sin contar con pruebas de que dar seguimiento a las alteraciones puede mejorar el pronóstico de las pacientes, nuestros hallazgos no deben considerarse aún para una práctica clínica de rutina”.
Actualmente, está en curso un estudio clínico de fase II del cáncer de mama triple negativo para evaluar si el uso de ctDNA en un entorno clínico mejorará el pronóstico de las pacientes.
Comparta su opinión sobre este artículo de fondo respondiendo nuestra breve encuesta.